 27.03.2024
27.03.2024
GMP-инспекции производителей ветпрепаратов в первом квартале 2024 года

В ежеквартальном обзоре представлена информация по инспектированию производителей ветеринарных препаратов на соответствие требованиям Правил надлежащей производственной практики (Good Manufacturing Practice, GMP), которое проводят специалисты Органа инспекции Федерального государственного бюджетного учреждения «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»).
Результаты инспектирования
Иностранные производители
Согласно реестру заключений, опубликованному на сайте Россельхознадзора 21.03.2024 г. [1], с начала этого года было выдано 7 заключений о соответствии требованиям Правил GMP. Эти заключения были сделаны в отношении площадок, расположенных в Аргентине, Венгрии, Китае, Нидерландах, Португалии, Румынии и США.
Анализ результатов инспектирования в тех странах, где было проведено наибольшее число российских инспекций, показывает следующие тренды:
- худшие результаты у производственных площадок, расположенных в Бразилии, США и Германии (более 80% отказов в выдаче заключения);
- лучшие результаты у производственных площадок, расположенных в Израиле и Словении(ни одного отказа в выдаче заключения).
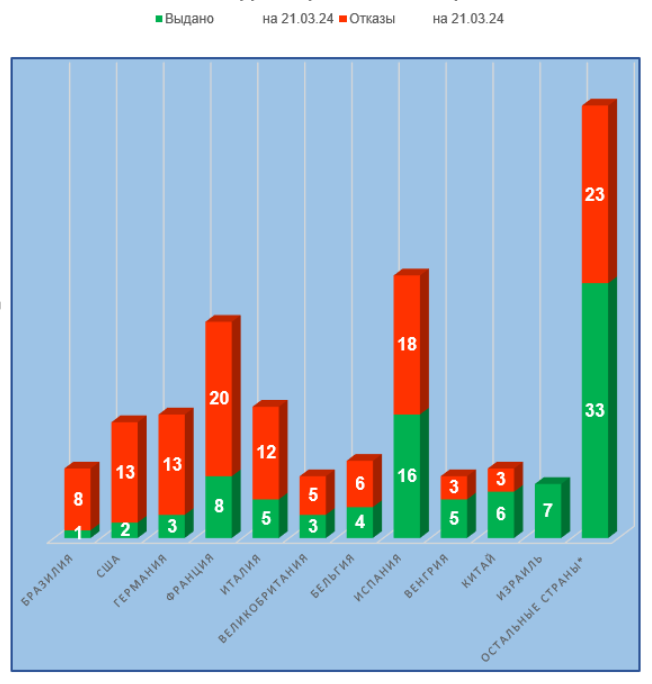
Результаты инспектирования производственных площадок, расположенных в Венгрии и Китае, несколько улучшились – процент отказов сократился до 38% и 33% соответственно. В первом квартале GMP-заключения получили площадки из Будапешта и Циндао.
Также немного снизился процент отказов по результатам инспекций, проведенных на площадках из США. Возможно, некоторые американские площадки стали более скрупулезно изучать Правила GMP ЕАЭС, утвержденные Решением Совета ЕЭК от 03.11.2016 г. № 77 [2] и проводить у себя внутренние аудиты на соответствие требованиям именно этих Правил.
Согласно реестру [1], к концу первого квартала количество действующих GMP-заключений возросло. На сегодняшний день зарубежные производители имеют 44 действующих GMP-заключения.
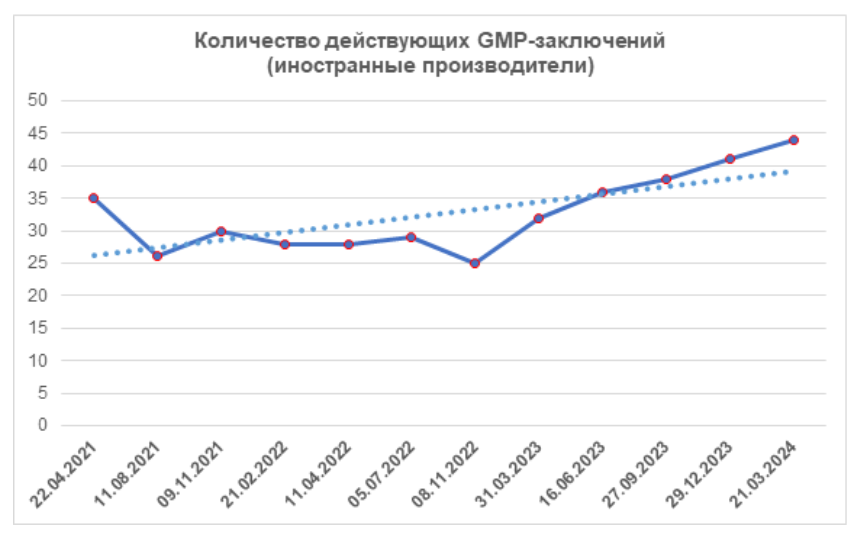
В соответствии с графиком проведения инспектирования, опубликованном на сайте ВГНКИ 21.02.2024 г. [3], на второй квартал 2024 годазапланировано 11 инспекций производителей ветеринарных препаратов, площадки которых расположены в Венгрии, Германии, Китае, Словении, США и Франции.
Российские производители
По информации Россельхознадзора [4], в настоящее время из 99 отечественных компаний 27 имеют сертификат GMP. Еще 14 производителей уже прошли процедуру подтверждения соответствия для дальнейшего получения заключения.
Прошедшие события и мероприятия
В первом квартале этого года прошло несколько событий и мероприятий, которые могли бы быть интересны производителям, готовящимся к инспектированию.
В начале февраля сообщество производителей лекарств и поставщиков PharmPRO провело бесплатный вебинар «Управление качеством: актуальные вопросы» [5]. Мероприятие было посвящено тонкостям составления регистрационного досье, нюансам регистрации укупорочных средств, а также критериям проведения аудита поставщика упаковочных материалов.
В своем выступлении международный эксперт Александр Александров подробно остановился на очном и дистанционном аудите, отметив плюсы и минусы каждого из них: «Дистанционный аудит зачастую более эффективен, чем очный, потому что в дистанционном аудите на тебя не влияет проверяемая сторона, она не оказывает влияния на твою оценку» [6].
В феврале группа депутатов Госдумы от ЛДПР внесла на рассмотрение палаты законопроект о приостановлении обязательства получать GMP-сертификат для ветеринарных лекарственных средств, ввозящихся из-за рубежа [7]. Согласно проекту, предлагается приостановить действие части 3 статьи 52 Федерального закона от 12.04.2010 г. № 61-ФЗ «Об обращении лекарственных средств» [8], которая предполагает, что ввод в гражданский оборот ввозимого в РФ лекарственного препарата для ветеринарного применения осуществляется при наличии заключения о соответствии производителя лекарственных средств требованиям Правил GMP, выданного уполномоченным федеральным органом исполнительной власти.
Оценивая данную инициативу, исполнительный директор ассоциации АВФАРМ Семен Жаворонковотметил [9]: «Что касается мнения отрасли, здесь все понимают, что на сегодняшний день альтернативы GMP-сертификации не существует – весь мир сертифицирует производителей на соответствие требованиям Правил GMP. В России также достаточно давно сложилось регулирование, когда без сертификата GMP нельзя вести нормальную деятельность, то есть регистрировать новые ветеринарные препараты и вносить изменения в досье на уже зарегистрированные. В этом смысле введение дополнительной проверки наличия у производителей российского GMP сертификата при вводе препаратов в гражданский оборот с 1 сентября прошлого года лишь обострило главную проблему – недостаточное число выданных сертификатов».
«Те предприятия, которые заинтересованы в сохранении своих позиций на рынке Российской Федерации, сделали все необходимое, чтобы пройти необходимые инспекции, или предпринимают эти усилия для ее прохождения, и таких предприятий немало», – в свою очередь комментирует ситуацию исполнительный директор Национальной ветеринарной ассоциации (НВА) Тимур Чибиляев[10].

Совет Госдумы рекомендовал внести законопроект на рассмотрение депутатов. Документ рассмотрят на пленарном заседании в мае 2024 года. До 9 апреля Комитет Госдумы по охране здоровья должен представить отзывы, предложения и замечания к законопроекту [11].
18 марта в Комитете Совета Федерации по аграрно-продовольственной политике и природопользованию состоялось заседание рабочей группы по законодательному обеспечению отечественного производства ветеринарных препаратов, кормов и кормовых добавок. По словам первого заместителя председателя Комитета Совета Федерации по аграрно-продовольственной политике Сергея Митина, принятие данной поправки может негативно сказаться на качестве и эффективности ветеринарных препаратов, безвредности для животных и может повлечь угрозу биологической безопасности страны. Свою оценку проекту дали заместитель директора департамента ветеринарии Минсельхоза России Ольга Николаичева и заместитель начальника Управления государственного ветеринарного надзора Россельхознадзора Анна Бабушкина. По итогам заседания рабочей группы сенаторами было принято коллективное решение не поддерживать данный законопроект [12].
Федеральное отраслевое издание «Ветеринария и жизнь» рассказало, какие законы и правила в сфере ветеринарии вступают в силу с марта 2024 года [13]. В частности, с 13 марта для стран ЕАЭС вводятся в действие единые «Правила регулирования обращения ветеринарных лекарственных средств на таможенной территории ЕАЭС», утвержденные Решением Совета ЕЭК от 21.01.2022 г. № 1 [14].
Ассоциация АВФАРМ представила сжатую сводку об изменениях, в том числе в области GMP-сертификации [15]: «В каждой стране ЕАЭС создадут национальные органы инспекции, которые будут проводить самостоятельные (для местных производителей) и совместные (для производителей за пределами ЕАЭС) проверки и подтверждать соответствие предприятий требованиям Правил GMP ЕАЭС [2]. Специалистов, имеющих необходимую квалификацию, объединят в общий реестр инспекторов ЕАЭС».
В феврале на базе Евразийской Академии надлежащих практик начал работу центр по обучению инспектората. Первым обучающим мероприятием нового центра стал интенсив «Валидация и квалификация на фармацевтическом производстве». Центр по обучению инспектората, созданный на базе Академии, стал первым в своем роде специализированным GMP-центром для фармацевтического инспектората в России и на всем пространстве ЕЭАС [16].
В марте на платформе Академии прошел очередной курс повышения квалификации «Подготовка аудиторов производства лекарственных средств»(заочная форма обучения с использованием дистанционных образовательных технологий) [17].
В первом квартале снова проводились бесплатные видео-встречи «Вопросы-Ответы GMP/GDP» с Александром Александровым. Например, в феврале обсуждалась тема «Документы и записи. Учет, обращение и обеспечение целостности данных».
Ближайшие события и мероприятия
16-18 апреля в Москве пройдет 22-я Международная выставка «Аналитика Экспо 2024» – единственная в России выставка лабораторного оборудования и химических реактивов для производственных и научно-исследовательских лабораторий различных отраслей [18].
17 апреля в рамках выставки будет организован «Форум для специалистов по контролю качества лекарственных средств», партнером которого выступит Учебный центр ДжиЭксПи. На форуме запланировано рассмотрение следующих тем: «Обзор требований к хранению готовой продукции», «Всесторонний взгляд на фармсубстанции: актуальные правовые вопросы и формирование регистрационного досье», «Методы контроля качества лекарственных средств на бактериальные эндотоксины и пирогенные вещества. Новые методы, направления и реактивы последних лет».
18 апреля в Москве состоится XIII Международный фармацевтический форум PharmPRO 2024. Это отраслевая площадка для общения и обмена опытом между производителями и поставщиками [19].
В рамках форума будет организовано несколько специальных сессий, в том числе сессия «Стабильное качество фармпрепаратов на каждом этапе». На этой сессии запланировано рассмотрение таких тем, как «Управление рисками при замене производителя исходного сырья и материалов на альтернативные», «Цифровизация процессов валидации», «Регистрационные аспекты в рамках GMP-инспекций» и др.
Производителям рекомендуется принимать активное участие в событиях и мероприятиях, связанных с GM(D)P, и тщательнее готовиться к инспектированию.
Представленный материал подготовлен с использованием данных, актуальных на 24.03.2024 г. В случае получения новых или дополнительных данных статья может быть обновлена.
Федеральное государственное бюджетное учреждение «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов», ФГБУ «ВГНКИ» – учреждение, уполномоченное на проведение инспектирования производителей лекарственных средств для ветеринарного применения, производство которых осуществляется за пределами Российской Федерации, на соответствие требованиям Правил GMP
Национальная ветеринарная ассоциация, НВА – некоммерческая организация, которая является коллаборацией ключевых биофармацевтических компаний
Ассоциация ветеринарных фармацевтических производителей АВФАРМ – ассоциация, представляющая на территории Российской Федерации интересы ведущих международных фармацевтических компаний-производителей лекарственных средств для ветеринарного применения (MSD Animal Health, Zoetis и Boehringer Ingelheim)
Ссылки:
- Россельхознадзор / Деятельность / Госуслуги / Выдача заключения о соответствии производителя (иностранного производителя) лекарственных средств для ветеринарного применения требованиям правил надлежащей производственной практики / Дополнительная информация для заявителя / Государственный реестр заключений о соответствии производителя (иностранного производителя) лекарственных средств для ветеринарного применения требованиям правил надлежащей производственной практики. URL: https://fsvps.gov.ru/ru/gosuslugi/zaklyuchenie-o-sootvetstvii (дата обращения 24.03.2024)
- Евразийский экономический союз / Решение Совета Евразийской экономической комиссии от 03.11.2016 г. № 77 «Об утверждении Правил надлежащей производственной практики Евразийского экономического союза». URL: https://docs.eaeunion.org/docs/ru-ru/01411921/cncd_21112016_77 (дата обращения 24.03.2024)
- ФГБУ «ВГНКИ» / Структура / Отдел инспекции производства на соответствие требованиям надлежащей производственной практики / График проведения инспектирования иностранных производителей на соответствие требованиям надлежащей производственной практики. URL: https://www.vgnki.ru/assets/2024/files/grafik–na–sajt-21022024.pdf (дата обращения 24.03.2024)
- Россельхознадзор / Россельхознадзор фиксирует почти трехкратный рост количества зарегистрированных отечественных ветеринарных препаратов. URL: https://fsvps.gov.ru/news/rosselhoznadzor–fiksiruet–pochti–trehkratnyj–rost–kolichestva–zaregistrirovannyh–otechestvennyh–veterinarnyh–preparatov/ (дата обращения 24.03.2024)
- PharmPRO / Вебинары / Управление качеством: актуальные вопросы. URL: https://events.pharmpro.pro/vebinar–quality-020224(дата обращения 24.03.2024)
- Фармпром / Экспертный материал / «Серые» зоны в управлении качеством на фармпроизводстве. URL: https://pharmprom.ru/serye–zony–v–upravlenii–kachestvom–na–farmacevticheskom–proizvodstve/(дата обращения 24.03.2024)
- ТАСС / ЛДПР предложила отменить обязательный сертификат соответствия для зарубежных ветлекарств. URL: https://tass.ru/obschestvo/20025125 (дата обращения 24.03.2024)
- Электронный фонд правовых и нормативно-технических документов / Федеральный закон от 12.04.2010 г. № 61-ФЗ «Об обращении лекарственных средств» (с изменениями на 30 января 2024 года). URL: https://docs.cntd.ru/document/902209774 (дата обращения 24.03.2024)
- Milknews / Мнения / Семен Жаворонков, АВФАРМ На сегодняшний день альтернативы GMP-сертификации не существует. URL: https://milknews.ru/interviu-i-blogi/zhavoronkov-minenie.html (дата обращения 24.03.2024)
- Сектор Медиа / Новости / Сельское хозяйство / Эксперты / Сельское хозяйство / «Продажа импортных препаратов без сертификата GMP навредит российским производителям». URL: https://sectormedia.ru/news/eksperty–selskoe–khozyaystvo/prodazha–importnykh–preparatov–bez–sertifikata–gmp–navredit–rossiyskim–proizvoditelyam/ (дата обращения 24.03.2024)
- Фармацевтический вестник / Новости / Регуляторика / Госдума рассмотрит в мае проект о продаже ветпрепаратов без специальной сертификации. URL: https://pharmvestnik.ru/content/news/Gosduma–rassmotrit–v–mae–proekt–o–prodaje–vetpreparatov–bez–specialnoi–sertifikacii.html (дата обращения 24.03.2024)
- Фармпром / Регуляторы фармрынка / Сенаторы не поддержали законопроект об отмене сертификата GMP для импортных ветпрепаратов. URL: https://pharmprom.ru/senatory–ne–podderzhali–zakonoproekt–ob–otmene–sertifikata–gmp–dlya–importnyx–vetpreparatov/ (дата обращения 24.03.2024)
- Ветеринария и жизнь / Законодательство / Какие законы и правила в сфере ветеринарии вступают в силу с 1 марта 2024 года. URL: https://vetandlife.ru/sobytiya/kakie–zakony–i–pravila–v–sfere–veterinarii–vstupajut–v–silu–s-1-marta-2024-goda/ (дата обращения 24.03.2024)
- Евразийский экономический союз / Решение Совета Евразийской экономической комиссии от 21.01.2022 № 1 «О Правилах регулирования обращения ветеринарных лекарственных средств на таможенной территории Евразийского экономического союза. URL: https://docs.eaeunion.org/Pages/DisplayDocument.aspx?s=%7Be1f13d1d-5914-465c-835f-2aa3762eddda%7D&w=9260b414-defe-45cc-88a3-eb5c73238076&l=%7B8a412e96-924f-4b3c-8321-0d5e767e5f91%7D&EntityID=32004 (дата обращения 24.03.2024)
- Зооинформ / Нвости / С 13 марта вступают в силу новые правила регулирования рынка ветпрепаратов для ЕАЭС. URL: https://zooinform.ru/v–avfarm–obyasnili–kak–s-13-marta–izmenitsya–regulirovanie–rynka–vetpreparatov/ (дата обращения 24.03.2024)
- Евразийская Академия надлежащих практик / Новости / На базе Евразийской Академии надлежащих практик начал работу центр по обучению инспектората. URL: https://gxp–academy.org/news/na–baze–evraziyskoy–akademii–nadlezhashchikh–praktik–nachal–rabotu–tsentr–po–obucheniyu–inspektorata/ (дата обращения 24.03.2024)
- Евразийская Академия надлежащих практик / Образовательная деятельность / Курсы ПК / «Подготовка аудиторов производства лекарственных средств». URL: https://gxp–academy.org/education/courses/podgotovka–auditorov–proizvodstva–lekarstvennykh–sredstv-/(дата обращения 24.03.2024)
- Аналитика Экспо / Деловая программа / Форум для специалистов по контролю качества лекарственных средств. URL: https://analitikaexpo.com/ru/agenda/bp_24/sessions24/Lecture2.2/ (дата обращения 24.03.2024)
- PharmPRO / XIII фармацевтический форум PharmPRO. URL: https://events.pharmpro.pro/forum-2024?roistat_visit=395104 (дата обращения 24.03.2024)
Теги: ветеринария, ветпрепараты, gmp инспекции
Количество показов: 538
Источник: https://pharmprom.ru/gmp-inspekcii-proizvoditelej-vetpreparatov-v-pervom-kvartale-2024-goda/
Материалы по теме:
- Минсельхоз: «Отечественные производители ветпрепаратов готовы к полному импортозамещению антибиотиков»
- ГК ВИК: Срок введения обязательной маркировки ветпрепаратов стоит увеличить
- Инновации в производстве лекарственных средств для ветеринарного применения
- Уникальный российский антибактериальный препарат “Фтортиазинон” выйдет в оборот в июне
- Правительство утвердило план мероприятий по реализации Стратегии развития Фарма-2030

















